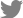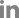|
 |
| J Korean Soc Cosmetol > Volume 28(6); 2022 > Article |
|
Abstract
Acetyl hexapeptide-8 (AH-8) is a well-known component of anti-aging products. AH-8 appears in a variety of cosmetic products, its skin penetration is sparsely studied and controversially discussed. This study investigated ampoule containing AH-8 as an active ingredient. The elasticity improving effect of 3% AH-8 ampoule was tested in vivo. To test the stability of the formulated ampoules, we performed the centrifugation, cycling and measured viscosity, and pH changes. 6 weeks-old female C3H mice were purchased from Orient Bio, Korea Inc. (Seongnam, Korea). After one week of acclimatization, the mice were randomly assigned to experimental groups (n=4 for each group); Control, UVB irradiation, Vehicle ampoule, and 3% AH-8 ampoule group. Irradiated with UVB to mouse skin, then 3% AH-8 ampoule were applied into irradiated sites for 6 weeks. Changes in the amount of TGF-β1 and collagen were measured using western blot. As a result, it was confirmed that the 3% AH-8 ampoule increased the expression of TGF-β1 and collagen. In summary, we showed that AH-8 ampoule had extremely high capability of improving elasticity when compared to vehicle ampoule containing ginkgo leaf and green tea extracts. This study revealed the efficacy of AH-8 for increasing skin elasticity and anti-aging in terms of a cosmetic active ingredient.
광노화는 장기간에 걸친 광노출로 인한 외적 피부 노화를 말하며 생리적 노화와는 차이가 있다. Ultravolet(UV) 노출로 인한 피부 세포의 손상 중 가장 주요한 변화는 진피 내의 콜라겐 손실이다. 피부의 생리적 기능에서 중요한 단백질인 콜라겐은 인간의 노화에 중요한 역할을 하는데 이는 피부 탄력에 관여한다. 콜라겐 합성에서 transforming growth factor-β(TGF-β)는 콜라겐 생성을 증가시키는 콜라겐 합성 유도 물질이라고 할 수 있다(Lin et al., 2017). UV에 의한 TGF-β 감소는 피부 손상, 콜라겐 섬유 구조의 문제를 초래하고, 진피 내의 콜라겐 손실이 나타나는 것으로 보고되고 있다(Quan et al., 2002). 또한 TGF-β는 단백질 분해효소인 matrix metalloproteinase(MMP) 유전자 발현을 방해하는데, MMP의 mRNA 및 단백질 발현을 억제한다(Gomes et al., 2012). 따라서 피부노화를 개선하기 위한 탄력 개선 효능에 관한 연구는 주로 콜라겐 생성 촉진에 집중되고 있다.
최근 소비자의 화장품 제품 선택 요인은 과거 브랜드 인지도에서 기능성, 목적성으로 변화되고 있으며 이에 따라 보습, 미백, 피부 주름 방지, 자외선 차단 및 흡수, 유해산소 제거, 콜라젠 합성 등 다양한 효능의 기능성 화장품이 개발되고 있다. 특히 피부과학과 화학공학의 결합에 기초하는 기능성 화장품 시장은 꾸준한 상승세를 이어갈 것으로 전망되고 있다(Jang et al., 2021). 화장품이 안티에이징 효과가 있으려면 피부재생 및 주름 개선 및 탄력증진 효능이 증명되어야 한다. 탄력개선의 효과 측정을 위한 평가법에는 TGF-β와 콜라겐의 변화를 in vivo 측면에서 정량하는 것이다.
Acetyl Hexapeptide-8(AH-8)은 보톡스와 유사한 작용 기전으로 주름 개선 효능을 가지면서 보톡스보다 안전한 생리활성 펩타이드로 주목받고 있다(Blanes-Mira et al., 2002; Hopple et al., 2015; Lungu et al., 2013). 특히 AH-8을 안면 주름에 적용하여 개선 효과를 보고한 연구는 다수가 보고되었으며(Blanes-Mira et al., 2002; Wisniewski et al., 2014), 눈꺼풀연축, 안검연축, 안검경련. 안륜근의 강직성 경련과 같은 얼굴 떨림 증상에도 적용하여 코스메슈티컬로서 보툴리눔 독소 테라피를 대체할 수 있는 탐색적 연구가 보고되었다(Lungu et al., 2013). 최근 보톡스가 피부질환 치료에 사용되기도 하는데 콜라겐이 병적으로 증가하는 켈로이드에 보톡스를 주사하면 켈로이드가 호전되는 것으로 보고되고 있다. 이상의 선행 연구는 AH-8이 신경에 작용하기도 하지만 콜라겐 합성에도 영향을 미칠 수 있다는 증거이다. 그러나 UVB에 의해 손상된 피부에 AH-8이 함유된 화장품을 적용했을 때 TGF-β와 콜라겐 발현 정도에 미치는 효과를 정량한 연구는 아직까지 미흡하다. 이 연구에서는 AH-8을 효능 원료로서 적용한 앰플을 제조하고, C3H 마우스 피부에 UV를 조사하여 광노화로 인한 피부손상에 AH-8 앰플이 피부 탄력 개선에 미치는 영향을 TGF-β와 콜라겐의 양적 변화를 측정하여 분석하였다.
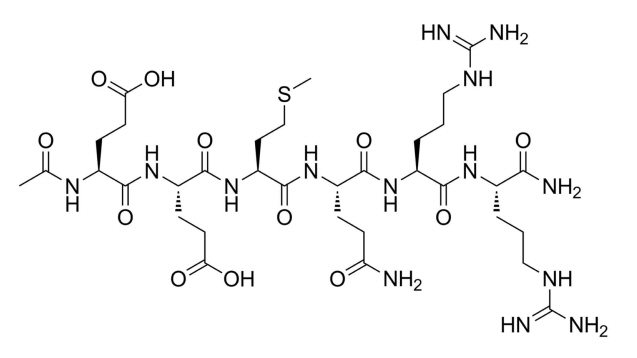
AH-8은 비드테크(DermaPepTM A610, Beadech, Ansan, Korea)에서 구입하여 사용하였다(Fig. 1).
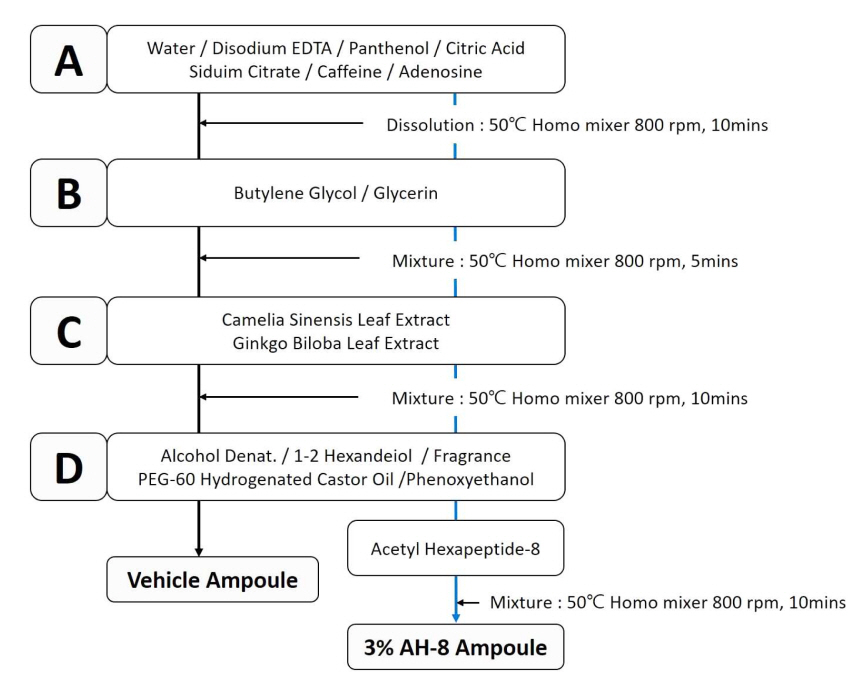
앰플의 제조 방법은 정제수, 점증제 등의 A 상(phase)의 원료를 계량하여 Homo mixer®(HM-U1.0, JPL Co, Seoul, Korea)로 50°C, 10분간 혼합하였다. B 상은 보습제와 용제를 계량하여 Homo mixer로 5분간 혼합하였다. 일반적으로 출시되고 있는 제품에 함유되는 대표원료로서 항상화 및 탄력개선에 효과가 있는 천연추출물 원료 Camellia Sinensis Leaf Extract와 Ginkgo Biloba Leaf Extract를 혼합하였다. 마지막으로 방부제, 향료 등의 원료를 계량하여 Homo mixer로 10분간 혼합하였다. A+B+C+D 상의 제조과정을 통해 베이스 기제에 해당하는 Vehicle 앰플을 제조하였다. Vehicle 앰플에 AH-8을 3%를 추가 하여 최종적으로 AH-8 앰플 시료를 제조하였다(Fig. 2).
Vehicle, 3% AH-8 앰플의 제형 안정도를 평가하기 위해 상온에서 원심분리 테스트를 하였다. 온도 변화에 대한 안정성을 평가하기 위해 사이클링 테스트를 하였고, 8주 동안 점도와 pH 변화를 측정하였다.
동물실험은 원광대학교 동물실험윤리위원회 심의 후(승인번호: WKU21-80) 시행하였다. 6주령의 C3H 마우스 암컷 16마리를 구매하였다(Orient Bio, Seongnam, Korea). 사육조건은 온도
22 ± 2°C, 습도는 50 ± 10%, 조명 12시간 명암으로 유지해 주었다. 마우스는 대조군을 포함하여 무작위로 4개 그룹(N=4)으로 할당하였다. AH-8 앰플에 의한 탄력효능을 평가하기 위해 두개의 시료를 Control(무처치)군과 UVB 조사군을 제외한 두 그룹의 C3H 마우스 등 피부 1×1 cm2 부위에 1 µL씩 매일 2회로 6주 동안 처치하였다. 그 후, 앰플이 피부에 흡수되는 시간을 고려하여 30분 후 UVB에 의한 광 노화를 유도하였다. Control군을 제외한 세 개 군의 마우스 등 피부에 UVB를 램프(UV Therapy System UV109, Waldmann, Villingen-Schwenningen, Germany)를 매주 주 1회 혹은 주 2회 동일 시간(10:00~11:00)에 조사하였다. 첫째 주는 1 minimal erythema dose(MED, 55~60 mJ/cm2) 2회, 둘째 주는 2 MED 2회, 셋째 주는 3 MED 1회, 넷째 주부터 여섯째 주까지 4 MED 1회로 조사하였다. 실험 기간 6 주 중 총 UV 노출량은 21 MED였다. 동물의 피부 채취 시 UV 손상에 의한 직접적인 영향을 받지 않도록 피부 채취 3일 전부터 UV를 조사하지 않았다.
6주 후 채취한 마우스의 등 피부를 액화 질소를 사용하여 미세분말까지 균질화한 후 lysis buffer[20 mM Tris-HCl(pH 7.5), 150 mM NaCl, 1 nM Na2EDTA 1 mM EGTA, 1% NP-40, 1% sodium deoxycholate, 2.5 mM sodium pyrophosphate, 1 mM β-glycerophosphate, 1 mM Na3VO4, 1 μg/ml leupeptin]에 혼합하여 용해하였다. 이를 얼음에 30분간 둔 후 12,000 rpm, 4°C에서 원심분리하여 상층액을 실험에 사용하였다. Sample을 12% SDS-PAGE를 이용해 전기영동하고 이를 membrane으로 이전시킨 후, 4% skim milk에서 방치하였다. 단백질이 이전된 membrane을 β-actin(1:5,000, Bioworld, Dublin, USA), TGF-beta 1(1:1,000, Abcam, Cambridge, UK), type I collagen(1:1,000, Abcam, Cambridge, UK)에 대한 1차 항체를 4°C에서 24시간 동안 반응시킨 후 TBST로 세척하였다. 이어 2차 항체(α-rabbit, 1:1,000, Abcam, Cambridge, UK)를 1시간 동안 반응시킨 후 TBST로 세척하였다. 이후 Membrane에 ECL kit(Amersham Pharmacia Biotech, Little chalfont, England)를 이용하여 필름에 옮겨 측정하였다.
제조한 앰플의 안정성 평가 결과는 다음과 같다. 먼저 원심 분리 테스트 후 각 앰플 시료의 분리 상태를 확인하였고 Vehicle, 3% AH-8 앰플 모두 성상의 분리가 없었다(Fig. 3-a). 또한, 5°C, 25°C, 50°C에서 각각 24시간 동안 저온과 상온, 상온과 고온을 반복하여(five-cycles) 사이클링 테스트를 한 결과에서도 Vehicle과 3% AH-8 앰플 모두 성상의 변화가 나타나지 않았다(Fig. 3-b).
앰플의 적절한 점도는 피부에 앰플을 도포할 때 편리성을 줄 수 있다. 또한 화장품의 안정성 측면에서 일정한 점도를 유지하여야 하므로 제조 후 점도의 변화를 8주간 측정하였다. 그 결과 Vehicle, 3%AH-8 앰플 시료 모두 5°C, 25°C, 50°C에서 점도가 안정적으로 유지되었다(Table 1).
제조한 앰플 시료들의 pH를 측정한 결과(Table 2)와 같다. vehicle과 3% AH-8 앰플의 상온 25°C에서의 pH는 5.87로 동일하였으며, 8주간 pH의 변화를 관찰한 결과 시간과 온도에 따른 pH 변화가 거의 나타나지 않아 제형 안정성을 확인하였다.
C3H 마우스 등 피부에 vehicle과 3% AH-8 앰플을 처치하고 자외선을 조사한 후 TGF-β1에 대한 발현 변화를 측정한 결과는 Fig. 4와 같다. Control(CTR)군을 기준으로 UVB를 6주 동안 총 21 MED 조사하였을 때 TGF-β1은 27% 감소하였다(p<0.01). 또한 Vehicle 앰플을 처치하고 UVB를 조사한 마우스 그룹의 피부에서도 TGF-β1이 43% 감소하였다. 그러나 3% AH-8 앰플을 처치하고 UVB를 조사한 마우스 그룹의 피부에서는 TGF-β1 20% 증가하여 통계적으로 유의한 차이를 확인하였다(p<0.01).
Transforming growth factor-beta1(TGF-β1)은 섬유아세포에 의한 콜라겐 분비에 강력한 자극제이다(Lijnen & Perov, 2002). 피부에서 TGF-β의 중심적 기능은 CTGF(connective tissue GF)의 SBE 표적 유전자 발현을 통해 type I 프로콜라겐 합성 및 분비를 유도하는 것이다(Quan et al., 2010). 또한, SMAD3 의존성 경로를 통해 MMP1 매개 콜라겐 발현을 억제한다(Yuan and Varga, 2001). 따라서 C3H 마우스 등 피부에 UVB를 조사한 후 광노화에 의한 TGF-β1의 감소를 확인하였으며, 대조 화장품에 해당하는 Vehicle 앰플 처치에서도 광노화에 의한 TGF-β1이 감소가 나타났다. 그러나 3% AH-8 앰플을 처치하였을 때 TGF-β1의 발현이 증가하여 3% AH-8 앰플이 피부에서 MMP1 매개 콜라겐 발현을 억제하고 프로콜라겐 합을 증진시켜 피부 손상을 억제함을 의미한다.
피부섬유아세포에서 생산되는 Collagen은 노화 과정 및 주름 형성에 밀접한 연관이 있으며 이는 피부탄력에 직결한다. 즉, Collagen과 같은 교원질들은 피부의 탄력을 유지하고 주름의 형성을 지연한다. 따라서 UVB에 의해 손상된 C3H 마우스 등 피부와 3% AH-8 앰플을 처치하고 자외선을 조사한 후 Collagen 발현변화를 측정하였다(Fig. 5). CTR군을 기준으로 UVB를 21 MED 조사하였을 때 Collagen은 30% 감소하였다(p<0.01). Vehicle 앰플을 처치하고 UVB를 조사한 마우스 그룹의 피부에서도 Collagen이 36% 감소하였다. 이는 UVB에 의한 피부 손상이 피부 탄력 손실에 직결됨을 알 수 있었다. 또한, 자외선만 조사한 마우스 그룹에 비해 Vehicle 앰플을 처치한 그룹에서도 Collagen 손실이 크게 나타났는데 이는 효능 원료를 사용하지 않은 화장품을 처치하더라도 자외선에 의한 피부 손상을 줄일 수 없음을 확인할 수 있는 결과이다. 그러나 3% AH-8 앰플을 처치하고 UVB를 조사한 마우스 그룹 피부는 Collagen이 48% 증가하여 통계적으로 유의한 차이가 나타났다(p<0.001). ICR 마우스를 대상으로 UVB를 조사하여(150 mJ/cm2) 피부를 손상시키고 Oenanthe javanica extract를 처치하여 콜라겐 types I and III를 정량한 선행연구 결과에서도 UVB 노출에 의해 피부의 콜라겐이 감소하였으나 피부 손상을 Oenanthe javanica extract가 UVB에 의한 피부 손상을 저해하는 것으로 발표하였다(Her et al., 2019). 선행 연구결과에서는 Oenanthe javanica extract가 UVB에 의한 피부 손상을 일부 저해하였으나 CTR 피부의 콜라겐 정량보다는 낮은 수치를 보였다. 이 연구에서는 3% AH-8 앰플이 UVB에 의한 피부 손상을 저해하였을 뿐 아니라 CRT보다 피부탄력 개선효능이 있음을 알 수 있었다.
이 연구에서는 탄력개선 효능이 예측되는 AH-8을 이용하여 앰플을 제조하고, 이에 대한 안정성 및 탄력개선 효능을 평가하였다. 그 결과, 먼저 안정성 측면에서 vehicle과 3% AH-8 앰플 모두 원심분리 테스트, 사이클링 테스트, 점도 및 pH 변화에 대한 제형 안정성을 확인하였다. In vivo에서, 탄력개선 효과를 평가하기 위해 C3H 마우스 피부조직을 채취하여 TGF-β1과 Collagen 1의 단백질 정량을 시행한 결과 3% AH-8 앰플 시료에서 TGF-β1과 Collagen 1의 발현이 증가하여 탄력개선 효과가 있음을 확인하였다. 서론에 제기하였던 바와 같이 보톡스펩타이드가 AH-8이 신경에 작용하기도 하지만 콜라겐 합성에도 영향을 미칠 수 있음을 확인하였다. 이 연구에서는 피부에 흡수가 쉬우며 탄력개선에 효과가 있는 항노화 펩타이드 화장품을 개발하고자 하였다. 결론적으로 Active 원료로 3% AH-8을 앰플에 적용하였을 때 화장품으로서 제형의 안정성을 확인하였으며, In vivo 측면에서 탄력개선 효과가 우수함을 알 수 있었다.
Fig. 3.
Centrifugation & Cycling test of 3% AH-8 ampoules.
Vehicle: Base ampoule does not contain anything 3% AH-8 ampoule: Vehicle containing 3% Acetyl Hexapeptide-8

Fig. 4.
TGF-β1 expression on UVB-induced C3H mouse skin. Data are presented by mean ± SD of three independent experiments performed in triplicate. Data were analyzed bu paired t-test. Levels of significance are indicated as ** for p<0.01. CTR : Control, UV : Treatment of UVB (total = 21 MED), Vehicle : Treatment of Vehicle ampoule and UVB, 3% AH-8 : Treatment of 3% AH-8 ampoule and UVB.
Fig. 5.
Collagen expression on UVB-induced C3H mouse skin. Data are presented by mean ± SD of three independent experiments performed in triplicate. Data were analyzed bu paired t-test. Levels of significance are indicated as ** for p<0.01, *** for p<0.001. CTR : Control, UV : Treatment of UVB (total = 21 MED), Vehicle : Treatment of Vehicle ampoule and UVB, 3% AH-8 : Treatment of 3% AH-8 ampoule and UVB.
Table 1.
Viscosity variation of ampoules (Unit : cps)
Table 2.
pH variation of ampoules
References
Blanes-Mira, C., Clemente, J., Jodas, G., Gil, A., Fernández-ballester, G., Ponsati, B., Gutierrez, L., Pérez-Payá, E., & Ferrer-Montiel, A. (2002 A synthetic hexapeptide (Argireline) with antiwrinkle activity. International Journal of Cosmetic Science, 24(5), 303-310. doi: 10.1046/j.1467-2494.2002.00153.x.


Her, Y., Shin, B. N., Lee, Y. L., Park, H. H., Kim, D. W., Kim, K. S., Kim, H., Song, M., Kim, J. D., Won, M. H., & Ahn, J. H. (2019 Oenanthe Javanica Extract Protects Mouse Skin from UVB Radiation via Attenuating Collagen Disruption and Inflammation. International Journal of Molecylar Science, 20(6), 1435-1447. doi.org/10.3390/ijms20061435.

Hoppel, M., Reznicek, G., Kahlig, H., Kotisch, H., Resch, G. P., & Valenta, C. (2015 Topical delivery of acetyl hexapeptide-8 from different emulsions: Influence of emulsion composition and internal structure. European Journal of Pharmaceutical Science, 68:27-35. doi: 10.1016/j.ejps.2014.12.006.

Gomes, L. R., Terra, L. F., Wailemann, R. A. M., Labriola, L., & Sogayar, M. C. (2015 TGF-β1 modulates the homeostasis between MMPs and MMP inhibitors through p38 MAPK and ERK1/2 in highly invasive breast cancer cells. BMC Cancer, 12:26.doi:10.1186/1471-2407-12-26.


Jang, M. A., & Lee, J. M. (2021 Research on domestic and international industrial trends of functional cosmetics. Journal of the Korean Applied Science and Technology, 38(2), 61-627. https://doi.org/10.12925/jkocs.2021.38.2.618.
Jo, H. W., Lee, K. H., & Kim, J. H. (2021 Preparation and Evaluation of the Effect of Acetyl Hexapeptide-8 Ampoule for Scalp Treatment. Asian J Beauty Cosmetol, 19(3), 435-444. doi:: https://doi.org/10.20402/ajbc.2021.0199.


Lijnen, P., & Perov, V. (2017 Transforming growth factor-beta 1-induced collagen production in cultures of cardiac fibroblasts is the result of the appearance of myofibroblasts. Methods & Findings in Experimental Clinical Pharmacology, 24(6), 333-344. doi:10.1358/mf.2002.24.6.693065.

Lungu, C., Considine, E., Zahir, S., Ponsati, B., Arrastia, S., & Hallett, M. (2013 Pilot study of topical acetyl hexapeptide-8 in the treatment for blepharospasm in patients receiving botulinum toxin therapy. European Journal of Neurology, 20:515-518. doi:10.1111/ene.12009.



Quan, T. H., He, T. Y., Kang, S., Voorhees, J. J., & Fisher, G. J. (2002 Ultraviolet Irradiation Alters Transforming Growth Factor β/Smad Pathway in Human Skin In Vivo. Journal of Investigative Dermatology, 119(2), 499-506. doi:10.1046/j.1523-1747.2002.01834.x.


Wisniewski, J. D., Elli, D. L., & Lupo, M. P. (2014). Facial rejuvenation: combining cosmeceuticals with cosmetic procedures. Journal of Cosmetic Dermatology, 94:122-126.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print