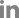|
 |
| J Korean Soc Cosmetol > Volume 27(4); 2021 > Article |
|
Abstract
The materials fermented with natural products have been used in a variety of cosmetic applications as a whitening, wrinkle and inflammatory agent. Prunus tomentosa fruits have been used as a traditional medicine for anti-oxidant and have been reported to possess anti-microbial properties. This study investigated the deramal bioactive properties of the Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF). The antioxidant activity of the PTF was measured by 1,1-diphenyl-2-picryl hydrazyl (DPPH) method. The cytotoxicity of human dermal fibroblast cell, murine macrophage cell line RAW 264.7 and B16-F10 melanoma cells were evaluated by sulforhodamine B (SRB) assay. Inhibitory effect of the PTF on nitric oxide (NO) prodction was evaluated by Griess Reagent System. The collagen synthesis was evaluated by using procollagen type-IC peptide (PIP) EIA kit. The tyrosinase activity, inhibitory effect of elastase and tumor necrosis factor-α (TNF-α) induced matrixmelloproteinase-1 (MMP-1) were also evaluated. It found that the PTF showed antioxidant activity without showing significant cytotoxicity in tested cells. The PTF were downregulated NO production in LPS-stimulated macrophages with nocytotoxicity (p<0.05). The PTF significantly induced collagen synthesis from the skin fibroblasts (p<0.05) and also dramatically inhibited MMP-1 activity (p<0.05). The PTF were inhibited activity of elastase and dramatically decreased melanin synthesis with inhibition of tyrosinase activity (p<0.05) and didn’t show cytotoxicity in B16-F10 melanoma cells. Therefore, the PTF showed bioactive properties on anti-oxidant, whitening, skin elasticity and anti-wrinkle efficacy. The PTF may be an appropriate choice for cosmetic products that aim to provide dermal bioactive effects.
중국 원산으로써 한국, 일본, 중국 등지에 분포하고 있는 앵두(Prunus tomentosa THUNB)는 앵두나무의 열매 앵도(櫻桃)라고도 한다. 앵도(櫻桃)는 영주(瓔珠: 옥구슬)와 비슷하게 연달아 열리고 모양이 복숭아와 비슷하므로 붙여진 이름이다(Kim, 2013). 또한, 꾀꼬리가 앵두를 먹기 때문에 “함도”라고도 하였다. 그리고 낭떠러지에서 양봉한 꿀과 같다는 뜻으로 “애밀(崖蜜)”이라고도 한다(Kim, 2013). 앵두를 언제부터 먹기 시작하였는지는 알 수 없으나 『제민요술(齊民要術)』에 재배의 기록이 나오는 것으로 미루어 우리 민족도 일찍부터 식용하였다고 한다(Cho, 2003). 우리나라의 문헌으로는 고려 시대의 『포은집(圃隱集)』에 등장하고, 고려 때부터 제사(祭祀)의 공물로 쓰거나 약재로 쓰였다(Han, 1996).
앵도(櫻桃)는 차하리, 천금이라고도 한다. 공 모양으로 6월에 붉게 익으며 새콤달콤한 맛이 난다. 주요 성분은 단백질·지방·당질·섬유소·회분·칼슘·인·철분·비타민(A·B1·C) 등이다(Hwang et al., 2003; Yoon & Park, 1985). 사과산·시트르산 등의 유기산이 들어 있으며, 붉은빛의 색소는 안토시안계로 물에 녹아 나온다. 혈액순환을 촉진하고 수분 대사를 활발하게 하는 성분이 들어 있다(Jang & Roh, 2004). 앵두는 자외선 차단과 멜라닌 색소 침착을 예방하고, 피부 미백에 효과적이다(Jeong, 2003; Hwang et al., 2003).
한편, 유산균은 프로바이오틱스로 세계적으로 그 유효성이 평가되고 있다(Kang, 2003). 프로바이오틱스는 장내 미생물의 균형을 향상해 건강을 증진시키는 미생물 첨가제의 의미로 쓰이고 있으며, 유산균 제제로 불린다. 대표적인 프로바이오틱스로는 Bifidobacterium, Lactobacillus, Lactococcus, Eneteroccus, Stretococcus 등이 있고, 대부분의 프로바이오틱스가 유산균들이며 일부 Bacillus 등을 포함한다(Fijan, 2014). 최근 경제적인 안정화와 삶의 질 향상 추구를 목적으로 건강관리와 식습관의 연관성에 대한 중요성이 증가하였고, 프로바이오틱스와 관련된 산업적 측면에서도 매우 큰 발전 가치가 있다고 보고하였다(Yang, 2014).
유산균 발효물은 당을 무산소 상태에서 분해하여 유기산을 생성하는 것으로 국내 다양한 소재들이 유산균 발효를 통하여 천연식물에 함유된 활성 성분 및 생리활성의 증가를 목적으로 활용되고 있다(Park & Kim., 2020; Lee et al., 2014; Yoo et al., 2019; Jeon et al., 2011; Jeong et al., 2019; Choi & Jung, 2017).
이에 앵두와 유산균의 발효로 생성된 물질에 대한 피부 생리활성 효과에 관한 연구는 미비한 상태로 본 연구자는 앵두나무 열매의 유산균 발효물을 이용하여 항산화, 항염, 미백, 주름 개선 등의 특성과 효능을 측정하여 피부 생리활성을 평가하고 유해성이 없는 성질의 천연 유래 식물성 성분을 활용한 화장품 소재 개발을 위한 기초자료로 활용하고자 한다.
세포배양에 사용한 DMEM(dulbecco′s modified eagle′s medium), FBS(fetal bovine serum), antibiotic-antimycotic solution, trypsin-EDTA는 Gibco제 GR급(Grand Island, NY, USA)을 사용하였으며, 세포 생존율을 측정하기 위해서 sulforhodamine B(SRB)와 dimethyl sulfoxide (DMSO)는 Sigma사에서 구매하였다(St. Louis, MO, USA). Cell culture dishes는 Falcon (BD Biosciences, Franklin Lakes, NJ, USA)에서 구매하여 사용하였다. 시료는 DMSO에 100 mg/ml로 용해하여 -20°C에 저장하면서 사용하였고, 0.1% DMSO는 negative control로써 사용하였다.
세포의 배양은 FormaTM Series II 3110 Water-Jacketed CO2 Incubators(Thermo Fisher Scientific Inc. Waltham, MA, USA)를 사용하였다. 세포수의 계산은 Turk형 혈구 계산기를 사용하였으며, 200배 배율에서 현미경(Olympus; Hamburg, Germany)을 사용하였다.
세포(cell)는 HDF(Human dermal fibroblast:인간 피부 섬유아 세포)를 CCD-1064SK(Momal human dermal fibroblast, ATCC CRL-2076, USA)로부터 구매하여 사용하였고, RAW 264.7 cell과 B16-F10 melanoma cells는 한국 세포주은행에서 분양받아 사용하였다. 구매한 세포(cell)를 DMEM/F12(3:1) 배지에 FBS(Fetal bovine serum) 10%, penicillin streptomycin 1%를 첨가하여 37°C와 5% CO2 조건에서 배양하여 실험에 이용하였다.
Man, Rogosa, and Sharpe(MRS) broth와 agar는 Gibco BRL(Grand Island, New York, NY, USA)을 사용하였다. Lactobacillus acidophilus는 비전 회사(Bision Corporation; Seongnam, Korea)를 사용하였고, 열매 발효를 위해 MRS broth를 고압증기멸균기(autoclave)를 사용하여 121°C에서 20분 동안 멸균한 뒤 유산균(S. thermophilus)을 3×106 colony-forming units per milliliter(CFU/ml) 되도록 접종하여 37°C에서 24시간 배양하여 종균을 얻었다. 이후 앵두 열매 5%, 종균 1%를 넣고 멸균되어 있는 MRS broth에 혼합한 뒤 37°C에서 24시간 배양하였다. 발효된 배양액을 동결 건조한 뒤에 냉동고에 보관하며 본 연구에 사용하였다(이를 PTF로 명명한다).
발효하는 사이 발효물의 유산균 수(colony)는 접종 후의 발효과정 동안 6시간 간격으로 측정하였다. 유산균 수의 측정은 MRS agar 배지를 이용하여 6, 12, 18, 24시간의 colony 수를 측정하여 평가하였다. 유산균 수는 CFU/ml로 나타내었다. 발효하는 과정 동안의 발효물 pH는 6, 12, 18, 24시간 간격에 맞추어 발효물을 채취하고, pH meter(Model 420; Thermo Orion, Minneapolis, MN, USA)를 이용하여 측정하였다.
세포독성 측정은 세포를 sulforhodamine B(SRB) 분석법으로 측정하였다(Lin et al., 1999). 즉, HDF(Human dermal fibroblast: 인간 피부 섬유아세포), RAW 264.7 cell, B16-F10를 96-well plate에 2×104 cells/well로 24시간 동안 배양한 뒤 배지를 제거하고, PTF을 1, 10, 50, 100 μg/ml의 농도로 처리해 배양하였다. 24시간 뒤 배지를 제거하고, 각 well에 아세톤 70%를 100 μl씩 첨가한 뒤 1시간 동안 -20°C에 방치하고, 아세톤을 모두 제거하였다. 60°C의 드라이 오븐(Dry oven)에서 건조한 뒤 1% (v/v) 아세트산에 용해한 0.4% (w/v) SRB 용액 100 μl를 첨가해 30분 동안 염색시켰다. 세포와 결합하지 않은 SRB 염색액을 1%(v/v)의 아세트산으로 여러 차례 세척한 다음 다시 건조시켰다. 각각의 well에 100 μl의 10 mM trysin을 mix한 뒤 560 nm에서 흡광도를 측정하였고, 결과에 대한 통계는 같은 조건으로부터 수행한 3번의 반복 실험 결과 수치의 평균값, 표준편차로 계산하여 값을 제시하였다.
PTF의 항산화 효과는 선행연구(Yen & Chen, 1995)에서 보고된 1,1-diphenyl-2-picrylhydrazyl(DPPH)의해 측정하였다. 즉, 앵두 발효물 1, 10, 50, 100 μg/ml의 농도를 가지는 50 μl에 0.3 mM DPPH 용액 50 μl를 혼합한 뒤 30분 동안 어두운 곳에서 반응시키고, 540 nm에서 microtiter plate reader를 이용하여 흡광도를 측정하였다. 항산화력은 실험군, 대조군의 흡광도 차이를 백분율(percentage)로 표시하였다.
RAW 264.7을 5×104 cells/well로 24-well plate를 접종한 뒤 24시간 동안 37°C의 인큐베이터에서 안정화했다. 배지를 교환하고, 내독소인 LPS를 10 μg/ml로 처리함과 동시에 시료를 처리하였다. 24시간 뒤 상층액을 취해 Griess reagent system(promega, Madison, WI) 키트(kit)을 이용하여 NO를 540 nm에서 흡광도를 측정하였다.
Fibroblasts에서 collagen 합성은 전에 보고된 방법에 따라서 procollagen type-IC peptide(PIP) EIA 키트(kit)에 의해 평가하였다(Parfitt et al., 1987). 즉, HDF는 96-well에 2×106 cells/well로 접종한 후, 각각 10 μg/ml의 PTF을 첨가한 후 37°C로 5% CO2 인큐베이터에서 배양하였다. Collagen synthesis 측정을 위해서 각 well에 100 μl antibody-peroxidase (POD) conjugate solution을 넣은 후, 연속적으로 PTF을 함유하는 용액, 혹은 표준 용액(640 ng PIP/ml)을 넣은 20 μl 배양액을 첨가하여 혼합하였다. Plate를 포일로 감싸고 37°C에서 3시간 동안 정치시켰다. 흡입기로 배지를 제거한 다음 400 μl phosphatebufferd saline(PBS)로 4회 세척한 다음 각 well에 100 μl substrate solution을 첨가하여 15분 동안 실온에서 반응시켰다. 각 well에 100 μl stop solution을 첨가하여 혼합한 후 plate reader(VERSAmax microplate reader; Molecular Devices, Palo Alto, CA, USA)를 사용하여 450 nm에서 흡광도를 측정하였다.
PTF의 엘라스틴 분해효소(Elastase) 저해 활성은 Moon방법에 의해 측정하였다(Moon et al., 2010). 돼지 췌장 엘라스틴 분해 효소(porcine pancreatic elastase; Sigma-Aldrich; St. Louis, MO, USA)의 저해 활성을 N-Suc-(Ala)3-nitroanilide의 기질로써 사용하며 410 nm에서 p-nitroanilin의 방출 양을 측정하였다. 5 mM N-Suc-(Ala)3-nitroanilide이 포함된 200 mM Tris-HCl buffer(pH 8.0)와 10 μg/ml의 분해효소를 혼합하고, 앵두열매 발효액을 최종 농도 각각 10, 20, 50, 100, 500 μg/ml가 되게 혼합하여 25°C에서 10분 동안 반응시키고, 410 nm에서 흡광도 측정을 하였다. 양성대조군으로 epigallocatechin gallate (EGCG)를 사용하였다(Kim et al., 2004). Elastase 저해율은 다음 식에 의해 산출되었다.
저해율(%) = [(ODConctrol − ODSample) / ODControl] × 100
50% 저해 농도(50% inhibitory concentration, IC50)는 doseresponse curves에 의해 산출하였다.
HDF 세포배양액에서 분비된 MMP-1 protein은 Matrix Metalloproteinase-1 Biotrack activity Assay Kit로 평가를 진행하였다(Gross et al., 1962). HDF 세포는 96-well에 2×105 cells/well, 10 μg/ml의 PTF, 10 ng/ml TNF-α를 처리하여 24시간 동안 37°C에서 배양하였다. 24시간 후, microplate reader를 사용하여 450 nm에서 흡광도를 측정하였으며, 표준 곡선은 세포에 의해서 분비되는 MMP-1 양의 정량을 사용하였다.
Tyrosinase 활성 측정은 Martinez-Esparza등에 의해 전에 보고된 방법에 따라 측정하였다(Martinez-Esparza et al., 1998). B16-F10 melanoma cells는 20 mM sodium phosphate(pH 6.8), 1%의 Triton X-100, 1 mM phenylmethane sulfonyl fluoride 혹은 PMSF로 용해시킨 후 14,000 rpm으로 15분간 원심 분리하였다. 각 상등 액의 표준 단백질 함량은 Bovine Serum Albumin(BSA)를 사용하는 Bradford assay에 의해서 결정하였다. Tyrosinase 활성은 50 mM phosphate buffer(pH 6.8), 2 mM LDOPA, 300 μg supernatant proteins를 포함하는 반응물 1 ml에서 결정하였다. 37°C에서 15분 반응액을 반응시킨 후 microplate reader를 사용해서 475 nm에서 흡광도를 측정하였다.
Tyrosinase 활성(%) = [(A-B)/C] × 100%
A: sample absorbance
B: blank absorbance
C: control absorbance
앵두 열매와 L. acidophilus와의 발효과정동안 L. acidophilus는 발효과정 동안 잘 자랐다. 앵두 열매 유산균의 발효과정 6, 12, 18, 24시간 동안 발효액을 통해 MRS agar 배지를 이용하여 유산균 수를 측정하였다<Fig. 1>. 발효액에서 L. acidophilus는 접종 후 7시간 이후 증식하기 시작하였고, 12시간 이후부터는 급격하게 증식하였다<Fig. 1>. 1일 후에 유산균 개체 수는 최고조에 달했으며, 8.6 log CFU/4 ml로 증식하였다<Fig. 1>.
피부의 pH는 각질층의 pH를 말한다. 적절한 피부의 pH는 4.5-5.5의 약산성을 의미하며, 산성막(acid mantle)과 같은 의미로 피부의 수분 증발을 방지함과 동시에 피부를 약산성으로 유지하고 유해물질이나 세균의 침입과 증식을 억제하는 피부 보호 기능을 한다(Kim & Hong, 2015).
PTF의 초기 pH는 7.2로 나타났고, 발효 전후의 pH는 4-6 사이로 낮아졌다<Table 1>. 발효 시간대별로 살펴보면 발효 12시간에는 pH가 6.2를 나타내었으며, 18시간에는 4.8, 24시간과 30시간에는 둘 다 4.4를 나타내었다. 따라서 발효 종료는 24시간에 이루어진 것으로 알 수 있었다. 유산균 발효물을 연구한 선행연구(Lim et al., 2019)에서 홍화 추출물의 발효물은 발효 기간의 경과에 따라 pH가 감소한다고 보고하여 본 연구와 유사한 경향을 보여주었다. 따라서 PTF의 24시간 발효 후의 유산균 개체 수는 108 CFU/ml로 나타났고, pH는 4.4로써 인체에 유용한 성분들이 생성된 것으로 보인다.
HDF, RAW 264.7, B16-F10 cell에 PTF을 1, 10, 50, 100 μg/ml의 농도로 세포독성을 측정의 결과, PTF은 대조군과 동일하게 모든 농도에서 약 100%의 생존율을 나타내 독성이 없는 것을 확인하였다. 유산균 발효물을 연구한 선행연구(Lee et al., 2014)에서 오미자 발효물은 100 μg/ml의 농도에서 피부섬유아세포에 대한 세포독성이 나타나지 않은 것과 비교하였을 때, PTF은 100 μg/ml의 최고 농도에서 100%의 세포 생존율을 나타냄으로써 이와 유사한 경향을 보였다. 따라서 PTF는 식품, 화장품 등에 적용하였을 때 독성이 없는 안전한 원료로 효과적인 물질인 것을 확인하였다.
항산화제에는 효소계열(superoxide dismutase, catalase, glutathion reductase 등)의 항산화제와 천연 항산화제(페놀성 화합물, flavone 유도체, ascorbic acid, carotenoids, glutathione 등), BHA(butylated hydroxyanisole), BHT(butylated hydroxytoluence), PG(propyl gallate) 등의 합성 항산화제가 있다(Kang et al., 2005). 합성 항산화제의 경우 과도하게 사용하면 독성이 있는 것으로 보고되어 있어 안전하고 우수한 항산화 효과를 가진 천연 항산화제의 개발이 활발하게 진행되고 있다(Masaki et al., 1995).
PTF의 항산화 효과를 DPPH 방법에 따라 측정한 결과는 Fig. 3과 같다. 양성대조군인 아스코르브산의 경우 0.2 mM에서 100.2%의 높은 항산화 활성을 나타내었고, PTF의 항산화 활성은 1, 10, 50, 100 μg/ml의 농도에서 각각 22.7%, 37.5%, 44.3%, 55.9%를 나타내어 농도 의존적으로 항산화 활성을 나타내었다. 특히 PTF은 10, 50 μg/ml의 농도에서 유의적인 항산화 활성을 나타냈으며(p<0.05), 100 μg/ml의 농도에서도 유의적인 항산화 활성을 나타내었다(p<0.01). 유산균 발효를 연구한 선행연구(Choi et al., 2017)에서 알 수 있듯 천연 유래 식물성 성분의 유산균 발효물은 항산화력이 있는 것으로 보고되어 본 연구의 항산화 활성 수치와 유사한 경향을 나타내었다. 따라서 PTF 자체의 항산화 효능이 있는 것으로 판단된다.
NO는 생체 내에서 신호 전달물질로 기체상 물질이며, 그 반응성이 매우 크다. NO는 다양한 생체 내 신호 전달 체계에서 매우 중요한 역할을 수행한다(Choi & Kim, 2000). 또한, 다량으로 존재하게 되면 각종 암이나 염증 발생에 관여한다. 특히 대식세포에서의 NO 생성은 염증 관련 인자를 활성화하는 역할을 한다(Nussler AK et al., 1993).
대식세포 RAW 264.7에 LPS (1 μg/ml)를 처리하여 NO 생성을 증가시키고(p<0.05), PTF을 각각 1, 10, 50, 100 μg/ml의 농도로 처리한 결과, NO가 농도 의존적으로 감소하였다(Fig. 4). 이러한 결과로 PTF는 NO 생성 저해효과에 유의적인 영향을 미치는 것으로 판단되며, 즉, 유산균 발효를 통한 성분이 대사 과정에서 염증을 억제시키도록 활성화하는 것으로 사료된다.
콜라겐은 피부 세포의 결합조직을 구성하며 섬유아세포(fibroblast)에서 생성되는 주요 조직 형성 단백질 성분으로 진피층의 약 90%를 차지하고 있다(Brinckmann et al., 1995). 피부의 결합조직인 콜라겐의 분해는 탄력 저하와 피부 주름 생성에 영향을 준다(Park et al., 2013). 콜라겐의 생합성과 분해, 조절은 피부의 노화 과정에서 가장 핵심적인 요소이다(Yuan et al., 2015).
피부 섬유아세포에 콜라겐 합성량을 조사한 결과, 양성대조군인 아스코르브산(L-AA)의 경우 0.2 mM에서 115.2%의 콜라겐 합성능을 보였다<Fig. 5>. PTF 처리군에서는 각각 10 μg/ml 37.5%, 50, 100 μg/ml 54.3%, 60.9%로 유의적인 증가를 나타내어(p<0.01) 콜라겐 합성능이 농도 의존적으로 증가하였다. 유산균 발효의 선행연구(Lee at al., 2014)에서 오미자 유산균 발효물은 콜라겐 생합성을 촉진한다고 보고하였다. 또한 대두발효추출물에서도 UV조사로 자극을 준 피부 섬유아세포에 콜라겐 합성량이 증가하는 것으로 확인하였다. 이는 PTF가 발효를 통하여 피부의 주름생성 예방, 노화 예방에 효과에 영향을 미칠 것으로 사료된다(Kim et al., 2019).
노화된 피부는 각질 세포층 지질의 양적 감소와 각질 세포 간의 지질 이중 막 수의 감소를 나타내며 진피층의 교원섬유나 기저 물질의 부족으로 섬유아세포의 활성이 떨어지고, 엘라스틴 섬유와 교원섬유의 양과 질이 감소하면서 피하지방층의 두께 감소로 피부 처짐과 주름 등 노화가 진행된다(Seong et al., 2008). 이때 엘라스틴을 분해하는 효소인 elastase의 활성은 피부의 탄력과 주름 형성을 일으키는 중요한 요인이 된다(Lee et al., 2008).
PTF의 엘라스틴 분해효소 저해 활성은 Table 2와 같다. PTF를 첨가했을 경우 엘라스틴 분해효소 50% 저해농도(IC50)은 32.47 μg/ml를 나타냈고, 양성 대조군(EGCG)의 50% 저해농도는 24.35 μg/ml를 나타냈다. 유산균 발효를 연구한 선행연구(Lee et al., 2014)에서 오미자 유산균 발효물의 엘라스틴 분해 효소 저해 활성 결과와 유사한 경향을 보였다. 또한 진생베리 발효액의 엘라스틴 저해활성을 확인한 결과, 1000 μg/ml에서 47.11±1.23%에서 저해활성을 보여 PTF가 상대적으로 낮은 농도에서 높은 저해효과를 나타내었다(Kim, 2020). 따라서 PTF의 elastase의 저해효과는 피부 결합조직 단백질을 보호하여 피부의 탄력과 노화 예방에 도움을 주는 것으로 사료된다.
피부는 나이가 들면서 여러 가지 환경적 자극원에 의해 피부의 여러 물질들을 분비한다. 진피세포는 세포 외 기질 단백질 분해 효소인 matrixmetalloproteinases를 분비하여 콜라겐, 엘라스틴 섬유 등의 기질 단백질을 분해한다. 콜라겐은 피부의 기질 구조 대부분을 차지하며 단백질 분해효소에 의해 분해되어 피부에 주름이 발생하고 탄력이 떨어지게 된다. 특히, MMP-1은 진피의 섬유아세포에 의해 생성되어 Type I, II, III으로 구성되어 있고, 이들은 콜라겐을 분해하여 노화를 촉진시킨다.
PTF로 배양된 세포 배양액를 첨가하여 MMP-1을 측정한 결과, Normal 81.7 ng/ml, TNF-α 98.7 ng/ml로 유의성 있게 증가하였음을 확인하였다(p<0.05). PTF을 1, 10, 50, 100 μg/ml로 처리 후 TNF-α를 처리한 결과 98.6, 87.6, 76.3, 72.1 ng/ml로 MMP-1의 활성을 저해하는 효과를 보였으며, 10 μg/ml이상에서 유의적인 감소를 나타내었다. 유산균 발효를 연구한 선행연구(Choi et al., 2017)에서 백련초 유산균 발효물의 MMP-1 저해활성 수치와 유사한 경향을 나타내었다. 또한 홍차 흑효모 발효물질의 연구에서 홍차 추출물보다 발효물질이 MMP-1 저해활성에 효과적이라는 보고가 있다(Kim et al., 2017). 이는 발효 물질이 MMP-1이 콜라겐에 특이적으로 작용하는 protease로서(Nagase et al., 1999). MMP-1의 발현 억제능을 나타내어, 항노화 효과에 긍정적일 것으로 사료된다.
피부색은 멜라닌 색소의 양에 의해서 결정된다(Boguniewicz et al., 2011). 멜라닌은 피부 표피의 기저층에 위치한 Malanocyte 내 소기관인 melanosome에서 티로신이 tyrosinase 효소에 의해 합성된다(Jung et al., 2009). 티로시나아제는 티로신과 페놀류를 산소에 의한 산화반응을 촉매하는 효소로, 여러 식물과 동물조직에도 존재하며, 멜라닌 색소 형성에 관여한다(Hwang et al., 2001).
B16-F10 cells에 양성대조군 arbutin 처리는 tyrosinase 활성을 9.8%로 유의성 있게 감소시켰고(p<0.01), PTF 1, 10, 50, 100 μg/ml로 처리한 결과 10 μg/ml 6.6%, 50과 100 μg/ml 9.4, 9.9%로 유의성 있는 감소를 나타내었다(p<0.01). 이는 유산균 발효물을 연구한 선행연구(Jeong, 2003)에서 보고되었던 상백피 추출물의 처리 농도에서 보다 유의적인 tyrosinase 저해율을 보여주었다. 따라서 PTF의 피부 미백 제품 등의 개발이 가능할 것으로 사료된다.
본 연구에서는 앵두 열매를 L. acidophilus로 유산균 발효물질 PTF로 세포독성, 항산화 활성, NO 저해 활성, 콜라겐 합성, 엘라스틴 분해 효소 저해 활성, MMP-1 저해 활성, 티로시나아제 활성에 대한 영향을 살펴본 후 다음과 같은 결과를 얻었다.
1. 앵두 열매와 L. acidophilus 유산균 발효는 유산균 개체 수가 발효 시작 24시간후 8.6 log CFU/ml로 증식하여 최고조에 달하여 종료 후 물질 PTF을 얻어 실험에 사용하였다.
2. 세포독성 실험결과, PTF 1, 10, 50, 100 μg/ml 농도에서 약 90% 이상의 생존율을 나타내어 독성을 나타내지 않아 피부에 안정적인 결과를 나타내었다.
3. 항산화 활성은 PTF 10, 50, 100 μg/ml의 농도에서 유의적인 항산화 활성을 나타내어, 추후 자외선이나 공기오염 등으로 산화물질에 의한 피부자극에 대하여 방어할 수 있는 것으로 나타내었다.
4. NO 저해활성은 PTF 1, 10, 50, 100 μg/ml의 농도로 처리한 결과, NO가 농도 의존적으로 유의적 감소를 나타내어 항염작용이 있는 것으로 사료되어 피부염증에 효과적인 결과를 나타내었다.
5. 콜라겐 합성능을 측정한 결과, PTF 10, 50, 100 μg/ml로 처리했을 때 농도 의존적으로 증가하였고, 유의적인 증가를 나타내어, 노화예방과 주름개선에 효과적인 결과를 나타내었다.
6. 엘라스틴(Elastase) 저해활성에서 50% 저해농도(IC50)은 PTF에서 32.47 μg/ml로 나타났고, 양성 대조군 EGCG의 저해 농도(IC50) 저해농도는 24.35 μg/ml로 나타내어, 주름개선과 탄력에 효과적인 결과를 나타내었다.
7. PTF은 TNF-α(Tumor necrosis factor alpha)를 10 μg/ml 이상으로 처리했을 때 MMP-1의 양이 유의적으로 감소하였다. 이는 콜라겐 분해효소인 MMP-1를 감소시킴으로써 노화예방에 효과적인 것으로 나타내었다.
8. B16-F10 cells에 PTF의 처리로 멜라닌 색소 형성에 관여하는 tyrosinase 활성을 유의적으로 감소시킴으로써 미백에 효과적인 것으로 나타내었다(p<0.01).
이상과 같은 결과로 볼 때 PTF은 본 연구에서 세포독성을 나타내지 않으며, 발효를 통하여 피부 생리활성 물질을 함유하여 항산화, 항염 효능 증가 및 멜라닌 생성 억제 효능, 피부 탄력과 피부 주름 개선 효과에 도움을 주는 천연 화장품 기능성 소재로 사용할 수 있을 것으로 나타내었다. 향후 PTF을 이용한 다양한 연구가 진행되고 연구 결과를 바탕으로 기능성 제품 개발로 이어져야 할 것으로 사료된다.
Fig. 1.
Growth of Lactobacillus acidophilus during fermentation of Prunus tomentosa fruits with Lactobacillus acidphilus (PTF) at 37°C.

Fig. 2.
Cell viability of human dermal fibroblast cells, RAW 264.7 and B16-F10 melanoma cells treated with Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF). Each column shows the mean±S.D of three independent experiments.
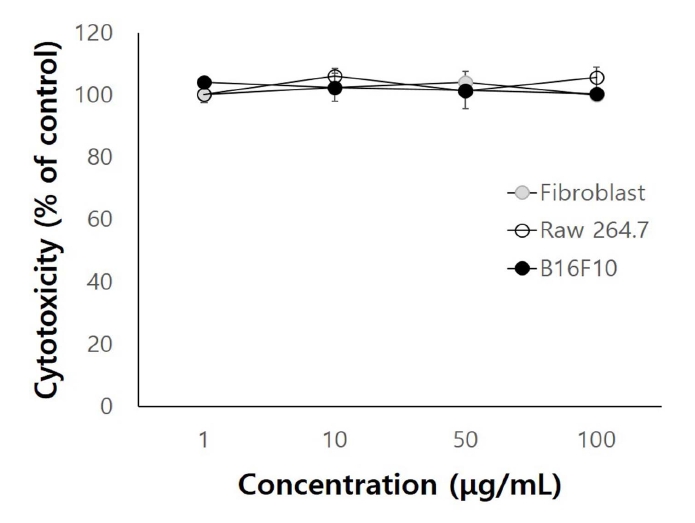
Fig. 3.
Antioxidant activity of Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF). Prunus tomentosa fruits fermented with Lactobacillus acidphilus were treated with 1, 10, 50, 100 μg/ml. Each column shows the mean±S.D of three independent experiments. AA; L-ascorbic acid (0.2 mM). *Significantly different from control (p<0.05). **Significantly different from control (p<0.01)
Fig. 4.
Inhibition of nitrite production by Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF) in LPS-stimulated RAW 264.7 cell. (A) Cells were co-incubated with the indicated concentrations of concentration of 1, 10, 50, 100 μg/ml and LPS (1 μg/ml) for 24 h. The culture supernatants were subsequently isolated and analyzed for nitrite production. Each column shows the mean±S.D of three independent experiments. #Significantly different from normal (p<0.05). *Significantly different from LPS (p<0.05). **Significantly different from LPS (p<0.01).

Fig. 5.
Collagen synthesis of human dermal fibroblast treated with Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF). Prunus tomentosa fruits fermented with Lactobacillus acidphilus were treated with 1, 10, 50, 100 μg/ml. Each column shows the mean±S.D of three independent experiments. AA; L-ascorbic acid (0.2 mM). #Significantly different from normal (p<0.05). *Significantly different from normal (p<0.05). **Significantly different from normal (p<0.01).
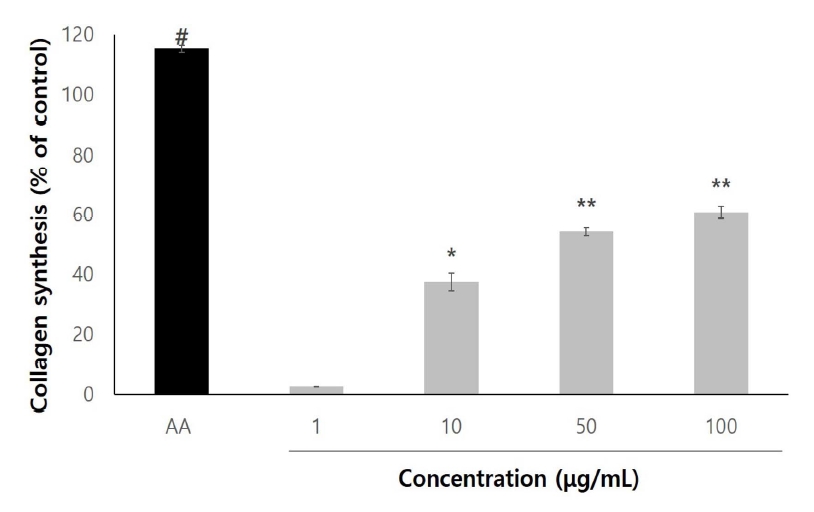
Fig. 6.
MMP-1 content in human dermal fibroblast incubated with Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF). Prunus tomentosa fruits fermented with Lactobacillus acidphilus were treated with 1, 10, 50, 100 μg/ml. Each column shows the mean±S.D of three independent experiments. #Significantly different from normal (p<0.05). *Significantly different from TNF-α (p<0.05). **Significantly different from TNF-α (p<0.01).
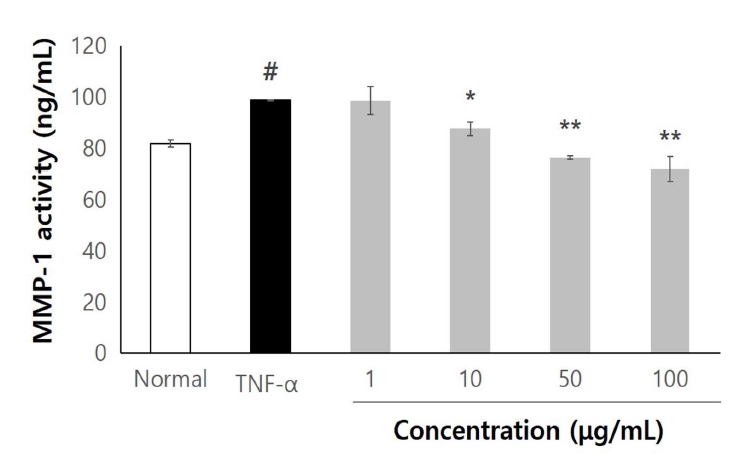
Fig. 7.
Inhibitory effect of Prunus tomentosa fruits fermented with Lactobacillus acidphilus (PTF) on tyrosinase activity in B16-F10 cells. Prunus tomentosa fruits fermented with Lactobacillus acidphilus were treated with 1, 10, 50, 100 μg/ml. Each column shows the mean±S.D of three independent experiments. #Significantly different from normal (p<0.05). *Significantly different from normal (p<0.05). **Significantly different from normal (p<0.01).

References
Cho, M. S. (2003). A study of intakes of vegetables in Korea. Korean Society of Food Culture, 18(6), 601-612.
Choi, H. J., & Jung, J. I. (2017). Evaluation of dermal bioactive properties of Opuntia humifusa (Backryeoncho) fruits fermented with Streptococcus thermophilus. Journal of the Korean Society of Cosmetology, 23(3), 515-520.
Choi, H. Y., & Kim, M. H. (2000). Substances attracting attention in skin research (5) Nitric Oxide. Korean Society for Investigative Dermatology, 7(3), 149-153.
Han, B. J. (1996). The historical study of Korean traditional funtional food. Journal of the East Asian Society of Dietary Life, 6(2), 235-255.
Hwang, H. S., Kim, J. M., Song, Y. A., & Jeon, Y. J. (2001). Inhibitory effect of ethanol extract and juice of the Korean cherry (Prunus tomentosa ThunBerg) on tyrosinase activity In vitro. Korean Journal of Food Science and Technology, 33(6), 760-763.
Hwang, H. S., Kim, J. M., Jeon, Y. J., Song, A. Y., & Park, H. S. (2003). Flavonoids and antimicrobial activity of the ethanol extract of Korean cherry (Prunus tomentosa Thun Berg). Journal of the Korean Society of Food Science and Nutrition, 32(6), 833-839.

Jang, K. H., & Roh, S. S. (2004). Depigmentation activity of many herb. Research Institute of Korean Medicine, 13(2), 289-302.
Jeon, J. M., Choi, S. K., Kim, Y. J., Jang, S. J., Cheon, J. W., & Lee, H. S. (2011). Antioxidant and antiaging effect of ginseng berry extract fermented by lactic acid bacteria. Journal of the Society of Cosmetic Scientists of Korea, 37(1), 75-81.
Jeong, K. O., Seol, C. H., Moon, K. H., Kim, D. G., Im, S. Y., & Lee, J. H. (2019). Physicochemical properties and antioxidant activity of Arctium lappa L. fermented with lactic acid bacteria. Journal of Chitin and Chitosan, 24(10), 8-15.

Jeong, Y. T. (2003). Active oxygen inhibition effect of cherry extract. Journal of the Korean Society of Cosmetology, 9(2), 137-147.
Jung, S. H., Ku, M. J., Moon, H. J., Yoo, B. C., Jeon, M. J., & Lee, Y. H. (2009). Inhibitory effects of fucoidan on melanin synthesis and tyrosinase activity. Journal of Life Science, 19(1), 75-80.

Kang, I. H., Cha, J. H., Lee, S. W., Kim, H. J., Kwon, S. H., Ham, I. H., Hwang, B. S., & Whang, W. K. (2005). Isolation of anti-oxidant from domestic Crataegus pinnatifida Bunge Leaves. Korean Journal of Pharmacognosy, 36(2), 121-128.
Kang, K. H. (2003). Lactobacillus properties and industrial use. The Korean Society of Food and Nutrition, 16(1), 86-92.
Kim, E. J., Shim, M. K., Jeong, A. R., & Kim, A. J. (2019). Antiphotoaging Effects of Fermented Soybean (Bio-Peptone®). Journal of the Society of Cosmetic Scientists of Korea, 45(1), 27-36.
Kim, I. C. (2020). Study on Cosmeceutical Activities from Fermented Ginseng Berry Extracts. Journal of the Korean Applied Science and Technology, 37(1), 28-37.
Kim, J. D. (2013). Literature on nature and effects of cherry [櫻桃]. Korean Agriciltural History Associastion, 12(1), 47-74.
Kim, N. J., & Hong, H. S. (2015). The correlation analysis of fluid Intake, skin hydration and skin pH of college students. Journal of Korean Biological Nursing Science, 17(2), 132-139.

Kim, Y. E., Yeo, M. A., Han, J. H., Lee, J. M., Jung, S. K., Jeong, H. A., Kim, S. H., & Lee, J. E. (2017). Aureobasidium pullulans Ferment of Black Tea for Anti-oxidation, Whitening and Antiwrinkle Effects. Journal of the Society of Cosmetic Scientists of Korea, 43(3), 265-271.
Lee, J. E., Kim, S. Y., Kim, S. Y., Oh, M. H., Yun, H. Y., Baek, K. J., Kwon, M. S., & Kim, D. S. (2008). Inhibitory effects of tannic acid on human skin fibroblast elastase activity. Journal of the Society of Cosmetic Scientists of Korea, 34(3), 217-223.
Lee, J. H., Kim, J. I., Choi, H. J., & Lee, J. H. (2014). Anti-wrinkle effect of Schizandra chinensis baillon rermented with Lactobacillus plantarum. Journal of the Society of Cosmetic Scientists of Korea, 40(4), 365-371.

Lim, M. J., Gu, Y. R., & Hong, J. H. (2019). Physicochemical properties and antioxidant activities of safflower (Carthamus tinctorius L.) extracts according to fermentation of lactic acid bacteria. Journal of Chitin and Chitosan, 24(1), 24-32.

Park, S. M., Kim, J. J., Jeong, K. Y., Han, S. K., Jeong, T. H., & Yun, M. Y. (2013). Antioxidant activity and inhibition of MMP-1 expression of Schizandrae fructus (Schizandra chinensis) extract. Korean Journal of Pharmacognosy, 44(1), 47-52.
Park, S. H., & Kim, J. Y. (2020). Effects of lactic acid fermentation of Bamboo shoot sheath on cosmetics usefulness. Journal of the Korean Society of Cosmetology, 28(2), 321-332.
Seong, E. J., Kim, H. Y., Ahn, M. S., Kim, H. Y., Jo, E. H., & Park, M. C. (2008). Treatment of wrinkles with oriental medicine. The Journal of Korean Oriental Medical Ophthalmology & Otolaryngology & Dermatology, 21(3), 184-199.
Yang, J. O. (2014). The current status and prospect of probiotic research and industrialization. Food Science and Industry, 47(4), 29-44.
Yoo, S. J., Chin, J. E., Oh, S. H., Ryu, M. J., & Hwang, K. T. (2019). Antioxidant activity in GABA lactic acid bacteria fermentation. Journal of Chitin and Chitosan, 24(3), 199-204.

Yoon, H. S., & Park, J. S. (1985). Lipid composition and protein pattern of Prunus Tomentosa thunberg seed. Korean Journal of Food Science and Technology, 17(4), 248-252.
Yuan, O. Y., Park, S. M., Lee, J. N., Choi, H. J., Lee, J. H., & Yun, M. Y. (2015). Research paper : Efficacy evaluation of deramal bioactive properties of the Chealbakgo extract. Journal of the Korean Society of Cosmetology, 21(6), 1158-1164.
Binic, I., Lazarevic, V., Ljubenovic, M., Mojsa, J., & Sokolovic, D. (2013). Skin ageing: natural weapons and strategies, Evidencebased Complementary and Alternative Medicine. 2013(1), 827248.


Boguniewicz, M., & Leung, D. Y. M. (2011). Atopic dermatitis: a disease of altered skin barrier and immune dysregulation. Immunology Review, 242(1), 233.

Fijan, S. (2014). Microorganisms with claimed probiotic properties: An overview of recent Literature. International Journal of Environmental Research and Public Health, 11(5), 4745-4767.



Garg, C., Khurana, P., & Garg, M. (2017). Molecular mechanisms of skin photoaging and plant inhibitors. International Journal of Green Pharmacy, 11(2), S218.
Gross, B., & Lapiere, C. (1962). Collagenolytic activity in amphibian tissue: a tissue culture assay. Proceedings of the National Academy of Sciences USA, 54:1197.
Martinez-Esparza, M., Jimenez-Cervantes, D., Lonzano, J. A., & García-Borrón, J. C. (1998). Mechanism of melanogenesis inhibition by tumor necrosis factor-alpha in B16/F10 mouse melanoma cells. European Journal of Biochemistry, 255(1), 139-146.


Sakaki, S., Atsumi, T., & Sakurai, H. (1995). Activeoxygen scavenging activity of plants extracts. Biological & Pharmaceutical Bulletin, 18(1), 162-166.


Moon, J. Y., Yim, E. Y., Song, G. P., Lee, N. H., & Hyun, C. G. (2010). Screening of elastase and tyrosinase inhibitory activity from Jeju Island plants. EurAsian Journal BioScience, 4(1), 41-53.

Mukherjee, P. K., Maity, N., Nema, N. K., & Sarkar, B. K. (2011). Bioactive compounds from natural resources against skin aging. Phytomedicine, 19(1), 64.


Nussler, A. K., & Billiar, T. R. (1993). Inflammation, immunoregulation, and inducible nitric oxide synthase. Journal of Leukocyte Biology, 54(2), 171-178.


Parfitt, A. M., Simon, L. S., Villanueva, A. R., & Krane, S. M. (1987). Procollagen type I carboxy-terminal extension peptide in serum as a marker of collagen biosynthesis in bone. Correlation with iliac bone formation rates and comparison with total alkaline phosphatase. Journal of Bone and Mineral Research, 2:427.





 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print